Sciex: Phân tích đồng thời dư lượng kháng sinh trong thủy sản
Dư lượng kháng sinh là các chất có khả năng gây nguy cơ cho sức khỏe của người tiêu dùng tồn tại trên các sản phẩm thực phẩm[1]. Hầu hết các hợp chất kháng sinh được quy định dựa trên dư lượng giới hạn tối đa (MRL) và một số ít hợp chất bị cấm sử dụng (ví dụ: Chloramphenicol[2]). Việc kiểm soát dư lượng kháng sinh có tầm quan trọng để đảm bảo an toàn của các sản phẩm thực phẩm khi đến tay người tiêu dùng.
Trước đây, các phương pháp phân tích thường được xây dựng riêng cho từng nhóm kháng sinh do sự khác biệt lớn về tính chất hóa lý và yêu cầu xử lý mẫu. Điều này khiến quy trình kiểm nghiệm mất nhiều thời gian, tốn kém hóa chất và hạn chế năng suất phân tích. Trong những năm gần đây, nhu cầu thị trường và áp lực từ các quy định an toàn thực phẩm đã thúc đẩy xu hướng phân tích đồng thời đa dư lượng kháng sinh – một giải pháp cho phép kiểm tra nhiều nhóm hợp chất khác nhau trong cùng một lần chạy máy. Phương pháp này không chỉ rút ngắn thời gian, giảm chi phí mà còn nâng cao hiệu quả kiểm soát chất lượng trong ngành thủy sản, đặc biệt với các thị trường xuất khẩu đòi hỏi tiêu chuẩn khắt khe.
1. Các phương pháp phân tích
1.1. Phương pháp tiêu chuẩn
Để đáp ứng nhu cầu của thị trường, các tổ chức quốc tế AOAC hay USDA đã ban hành các tiêu chuẩn về phương pháp phân tích dư lượng các hợp chất kháng sinh trên các nền mẫu thực phẩm.
Theo các tiêu chuẩn công bố, hệ thống sắc ký lỏng ghép nối đầu dò khối phổ hai lần (LC-MS/MS) là một phương pháp mạnh mẽ, phù hợp phân tích đa dư lượng kháng sinh trong thực phẩm, đáp ứng về độ nhạy, độ chính xác và thời gian thu được kết quả nhanh chóng.
Theo AOAC 2020.04, “Screening of 154 Veterinary Drug Residues in Foods of Animal Origin Using LC–MS/MS”, tùy thuộc vào tính chất hóa lý, phương pháp phân tích dư lượng kháng sinh được chia thành 4 nhóm: Multiclass (Stream A), b-Lactams (Stream B), Aminoglycosides (Stream C), Tetracycline (Stream D) với 4 phương pháp xử lý và phân tích mẫu.[1] USDA cũng đưa ra các phương pháp phân tích với từng nhóm kháng sinh cụ thể. [3], [4], [5]
1.2. Phương pháp phân tích trên sản phẩm của SCIEX
Theo xu hướng của thị trường, hãng SCIEX cũng đã công bố các phương pháp phân tích kháng sinh trên các dòng sản phẩm LC-MS/MS. Phương pháp phân tích kháng sinh nhóm Nitrofuran bao gồm Furazolidone, Furaltadone, Nitrofurazone và Nitrofurantoine trên nền mẫu tôm và thịt bằng cách tạo dẫn xuất trong giai đoạn xử lý mẫu và thực hiện phân tích trên dòng máy AB SCIEX 3200 Series đạt được giá trị LOQ ~ 0.1 ng/mL (SEM) và ~ 0.02 ng/mL đối với AOZ, AHD, AMOZ.[6]
Phân tích đồng thời kháng sinh Chloramphenicol và Tetracycline trong nền mẫu thực phẩm với phương pháp chiết QuEChERS và phân tích trên hệ thống SCIEX Triple QuadTM 3500 với cả 2 chế độ ion hóa âm dương trong cùng một phương pháp chạy mẫu. Kết quả thu được khoảng tuyến tính 0.005-100 ng/mL cho Chloramphenicol và 0.1 – 100 ng/mL cho Tetracyclines với hệ số hồi quy tuyến tính R2 > 0.997. [7]
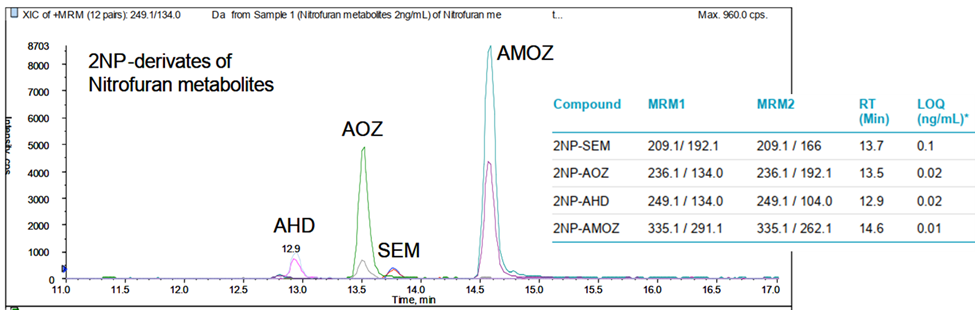
Hình 1. Sắc ký đồ kháng sinh nhóm Nitrofuran trên hệ thống AB SCIEX 3200 Series
Nhìn chung:
các phương pháp xử lý và phân tích kháng sinh được thực hiện theo từng nhóm riêng rẽ. Hiện nay, phương pháp phân tích đồng thời dư lượng kháng sinh vẫn là một thách thức lớn đối với các nhà phân tích hóa học. Sự đa dạng về đặc tính lý hóa của các nhóm kháng sinh là một trở ngại lớn để đạt được hiệu suất phân tích tốt cho các hợp chất được phân tích đồng thời.[8]
Trong những năm gần đây, xu hướng chuyển từ phân tích riêng lẻ các nhóm sang phương pháp phân tích đa nhóm kháng sinh, do đó cần phải có một thiết bị phân tích đủ mạnh để đáp ứng được độ nhạy và độ ổn định.
2. Phương pháp phân tích đồng thời các hợp chất kháng sinh
Giải pháp của Việt Nguyễn kết hợp với Công nghệ của SCIEX Triple QuadTM 5500+ LC-MS/MS system – QTRAP Ready
Việt Nguyễn tiếp cận bài toán phân tích kháng sinh trên nền mẫu thủy sản với mục tiêu giảm thiểu quy trình xử lý mẫu bằng cách gom các nhóm kháng sinh có cùng tính chất hóa lý và tối ưu quy trình phân tích mẫu không làm sạch và làm giàu nhờ vào công nghệ của thiết bị SCIEX Triple QuadTM 5500+ LC-MS/MS system – QTRAP Ready. Quy trình phân tích được thực hiện với 20 hợp chất kháng sinh thuộc 6 nhóm Quinilone, Sulfalamide, Nitrofuran, Phenicols, Triphenylmethane và Tetracycline. Phương pháp phân tích được triển khai trên nền mẫu thủy sản với 2 phương pháp xử lý mẫu cho 6 nhóm kháng sinh.
2.1.Tính chất lý hóa của các nhóm kháng sinh
Sulfonamides (SA)
Sulfonamides (SA) là dạng dẫn xuất của sulfanilamide, sự thay đổi đặt tính lý hóa tùy vào sự gắn hoặc thay thế các nhóm chức khác nhau trong nhóm amido hoặc sự thay thế trong nhóm amino. Mặc dù SA có tính chất lưỡng tính và giá trị pKa trong khoảng 4.8 – 8.6, SA thường hoạt động giống như các acid hữu cơ yếu và dễ tan trong dung dịch kiềm hơn là acid. [8]
Tetracycline (TC)
Tetracycline (TC) tồn tại 3 dạng trong tự nhiên là Chlotetracycline (CTC), Oxytetracycline (OTC) và desmethyltetracycline. Đa phần, các hợp chất TC tan trong nước, có tính phân cực mạnh và có tính base kém với giá trị pKa từ 3.2 – 9.8. Nhóm tetracycline có khả năng tạo phức tốt vì vị trí C1 và C11 có 2 nhóm ketone.[8]
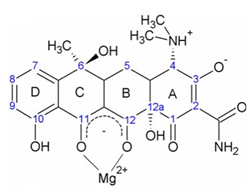
Hình 2. Phức chất của tetracycline với kim loại Mg2+ [9]
Quinolones
Quinolones là hợp chất kháng sinh có cấu trúc đa dạng, đa phần các chất có nhóm carboxylic ở vị trí thứ 3 làm cho các hợp chất có tính acid. Tuy nhiên, các quinolone 7-piperazinyl thậm chí còn có nhóm thế base. Nhờ vào các nhóm thế khác nhau, các quinolone sẽ có tính chất lý hóa khác nhau về tính chất lưỡng tính, cation hoặc anion. Nhóm quinolone có khả năng tạo phức với kim loại Ca2+, Zn2+, Fe2+,… hoặc Al3+, Fe3+ ở vị trí nhóm carbonyl và carboxyl.[10]
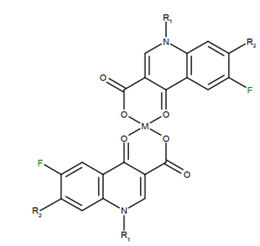
Hình 3. Cấu trúc chung của 1:2 (kim loại: phối tử) quinolone chelate với cation hóa trị hai[11]
Nitrofuran
Nitrofuranlà những hợp chất kháng sinh có chứa cấu trúc vòng 5-nitrofuran. Các gốc nitrofuran chuyển hóa nhanh chóng thành các chất liên kết với protein. Do liên kết công hóa trị với preotein trong mô tế bào, việc chiết xuất bằng dung môi sẽ không hiệu quả, thay vào đó cần phải có bước thủy phân acid để tách các chất ra khỏi nền mẫu.[12]
Amphenicols
Amphenicols tiêu biểu là hợp chất Chloramphenicol. Đây là một dẫn xuất của nitrobenzene trung tính, tan trong Lipid và có thể được sử dụng như một base tự do hoặc ester. [8]
Triphenylmethane dye
Triphenylmethane dye là những loại thuốc nhuộm mà trong đó một nguyên tử cacbon trung tâm được liên kết với hai vòng benzen và một nhóm p-quinoid (chromophore). Các auxochrome là – NH2, NR2 và –OH.[8]
2.2. Tại sao phân tích đồng thời kháng sinh lại khó?
2.2.1. Đặc tính hóa lý
Sự khác biệt về đặc tính lý hóa của các nhóm kháng sinh là một trở ngại lớn cho việc phân tích đồng thời trong cùng điều kiện xử lý và phân tích mẫu. Vì vậy, đa phần các tiêu chuẩn hiện nay đều xây dựng phương pháp phân tích cho từng nhóm kháng sinh cụ thể.
Các hợp chất kháng sinh có thể bị phân hủy ở nhiệt độ cao (như tetracycline) hoặc phải tạo dẫn xuất để có thể lưu giữ và phân tích tốt trên LC-MS/MS (nhóm nitrofuran). Do đó, việc phân tích đồng thời các hợp chất này là điều thực sự khó khăn khi phân tích đồng thời các chất thuộc các nhóm này.
2.2.2. Nền mẫu
Nền mẫu cũng là một yếu tố cần lưu ý, vì đa phần các nền thủy sản đều giàu béo, đòi hỏi phải cần qua bước làm sạch (bằng PSA, C18,…) để giảm thiểu ảnh hưởng nền. Điều này cần phải cân nhắc khi sử dụng, vì một số hợp chất làm sạch có thể gây mất chất phân tích. Ví dụ, sử dụng PSA khi làm sạch mẫu cho hiệu suất thu hồi thấp hơn, có thể là do PSA không chỉ hấp phụ các chất gây nhiễu mà còn hấp phụ luôn cả các hợp chất kháng sinh.[13] Do vậy, phương pháp xử lý mẫu không qua bước làm sạch được hướng đến.
Các hợp chất như nhóm Tetracycline và Quinolone có khả năng tạo phức với kim loại, điều này dẫn đến khó khăn trong quá trình phân tích định lượng. Vì vậy, trong bước chiết các hợp chất thuộc nhóm này cần phải thêm EDTA – một chất tạo phức với các ion kim loại, giúp cải thiện hiệu suất thu hồi của phương pháp. Tuy nhiên, EDTA khi sử dụng để chiết đồng thời với các nhóm chất kháng sinh khác như Sulfadimethoxine lại cho hiệu suất thu hồi thấp hơn đáng kể.[14]
2.3. Giải pháp gom quy trình phân tích kháng sinh
Dựa và các đặt tính lý hóa và nhu cầu phân tích. Phương pháp phân tích 6 nhóm kháng sinh được chia làm 2 quy trình xử lý mẫu:
+ Nhóm Tetracycline và nhóm Quinolone được chiết với 0.1% acid formic trong Methanol với sự có mặt của EDTA để tạo phức với các kim loại có trong nền mẫu. Dịch chiết được lọc và tiêm thẳng vào máy.
+ Các nhóm còn lại được gom lại chung thành một quy trình xử lý mẫu. Bao gồm việc tao dẫn xuất của nhóm nitrofurane với 2-Nitrobenzaldehyde trong môi trường acid HCl. Hydroxylamine là 1 chất có tính khử, ngăn ngừa sự chuyển đổi oxy hóa – khử của các hợp chất nhóm triphenylmethane dye. Mẫu sau đó được ủ nhiệt độ và chiết bằng dung môi Ethyl acetate trong môi trường pH=7 (điều chỉnh bằng K2HPO4 1M). 5 mL Dịch chiết được thổi khô và hòa tan với 1 mL pha động sắc ký và tiêm vào máy.
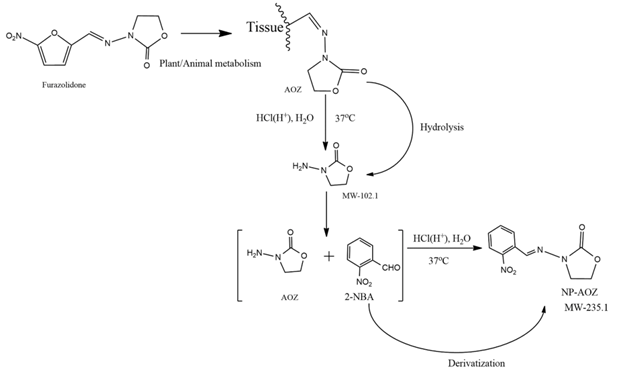
Hình 4. Dẫn xuất của hợp chất Furazolidone (AOZ)[15]
3. Kết quả phân tích
Giới hạn phát hiện của phương pháp (LOD) đạt được đều ở mức thấp khoảng 1 ug/kg cho nhóm tetracycline và từ 0.01-0.1 ug/Kg cho các nhóm còn lại với khoảng tuyến tính được được trình bày trong bảng 1.
| Nhóm | Tên hợp chất | LOD (mg/Kg) | Khoảng tuyến tính (mg/Kg) |
| Quinilone | Ciprofloxacine | 0.1 | 0.1-20 |
| Enrofloxacine | 0.1 | 0.1-20 | |
| Norfloxacine | 0.1 | 0.1-20 | |
| Ofloxacine | 0.1 | 0.1-20 | |
| Sulfalamide | Sulfachloropyridazine | 0.1 | 0.1-20 |
| Sulfadiazine | 0.1 | 0.1-20 | |
| Sulfamethoxazole | 0.1 | 0.1-20 | |
| Sulfamethazine | 0.1 | 0.1-20 | |
| Sulfadimethoxine | 0.1 | 0.1-20 | |
| Nitrofuran | AOZ | 0.02 | 0.02-20 |
| AMOZ | 0.02 | 0.02-20 | |
| AHD | 0.02 | 0.02-20 | |
| SEM | 0.02 | 0.02-20 | |
| CAP | Chloramphenicol | 0.01 | 0.01-20 |
| Triphenyl methane | MalachiteGreen | 0.1 | 0.1-20 |
| Leuco Malachite Green | 0.1 | 0.1-20 | |
| Crystal violet | 0.1 | 0.1-20 | |
| Leuco Crystal violet | 0.1 | 0.1-20 | |
| Tetracycline | Doxycycline | 1 | 1-200 |
| Oxytetracycline | 1 | 1-200 | |
| Tetracycline | 1 | 1-200 |
Với kết quả đạt được, quy trình phân tích đã được áp dụng trên nền mẫu thực tế và thành công tại nhà máy thủy sản NTFS (Cần Thơ) với kết quả đạt được tốt và đáp ứng được nhu cầu của nhà máy. Quy trình phân tích mẫu đáp ứng được ngưỡng giới hạn cho phép (MRL), khoảng tuyến tính với giá trị hệ số tương quan R2 > 0.99 với giới hạn phát hiện (LOD) thấp. Phương pháp cũng đáp ứng tốt về độ đúng và độ chính xác của kết quả kiểm nghiệm và nâng cao năng suất phân tích mẫu.
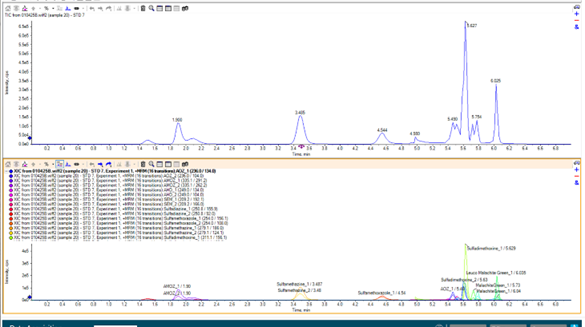
Hình 5. Sắc ký đồ TIC và XIC của các hợp chất kháng sinh phân tích trên hệ thống LC-MS/MS SCIEX Triple Quad 5500+ QTRAP Ready
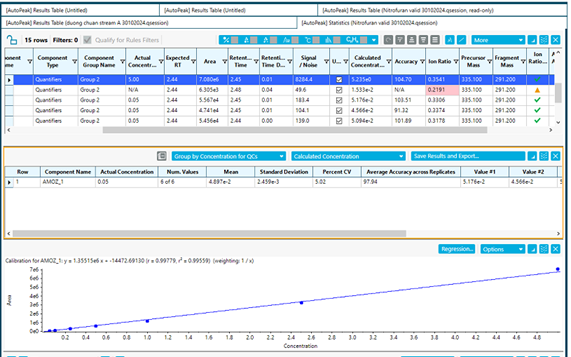
Hình 6. Đường chuẩn của AMOZ với hệ số tương quan R2 = 0.99559
4. Kết luận
Quy trình phân tích 20 hợp chất kháng sinh trên nền mẫu thủy sản thuộc 6 nhóm Quinilone, Sulfalamide, Nitrofuran, Phenicols, Triphenylmethane và Tetracycline trên thiết bị SCIEX Triple QuadTM 5500+ LC-MS/MS system – QTRAP Ready đã đạt được:
– Phương pháp phân tích đã giảm thiểu còn 2 quy trình xử lý mẫu.
– Phương pháp bỏ qua bước làm sạch, vì vậy đã giảm thiểu được thời gian phân tích mẫu và chi phí hóa chất.
– Giới hạn phát hiện của phương pháp thấp, đủ đáp ứng phát hiện và định lượng các hợp chất kháng sinh vượt ngưỡng MRLs.
– Quy trình được triển khai tại nhà máy thủy sản NTFS và đạt được yêu cầu mục tiêu của nhà máy về LOD và tăng công suất phân tích mẫu.
Tài liệu tham khảo
[1] A. Desmarchelier et al., “Screening of 154 Veterinary Drug Residues in Foods of Animal Origin Using LC-MS/MS: First Action 2020.04,” J AOAC Int, vol. 104, no. 3, pp. 650–681, May 2021, doi: 10.1093/jaoacint/qsaa168.
[2] “10-bnnptnt-pl-2”.
[3] U. Fsisd, “CLG-AMG4.02. Screening for Aminoglycosides by LC-MS-MS.”
[4] U. Fsis, “CLG-MRM3.02 – Screening and Confirmation of Animal Drug Residues by UHPLC-MS-MS.”
[5] U. Fsis, “CLG-BLAC.03 Screening and Confirmation of β-Lactam Antibiotics by HPLC-MS/MS.”
[6] “A Rapid iMethodTM Test for the Quantitation of Nitrofuran Metabolites in Meat and Shrimp, Liver and Honey iMet h od TM Test,” 2010. [Online]. Available: www.sigmaaldrich.com
[7] A. Sharma, S. Kapil, ; M Chandrasekar, ; Anoop Kumar, M. Pillai1, and J. Stahl-Zeng, “Rapid, Sensitive, Quantitation method for Chloramphenicol in Meat using SCIEX Triple QuadTM 3500 LC-MS/MS System,” 2002. [Online]. Available: http://fao.org/agriculture/dairy-gateway/meat-production/en.
[8] S. C. Barros, A. S. Silva, and D. Torres, “Multiresidues Multiclass Analytical Methods for Determination of Antibiotics in Animal Origin Food: A Critical Analysis,” Feb. 01, 2023, MDPI. doi: 10.3390/antibiotics12020202.
[9] G. J. Palm et al., “Specific binding of divalent metal ions to tetracycline and to the Tet repressor/tetracycline complex,” Journal of Biological Inorganic Chemistry, vol. 13, no. 7, pp. 1097–1110, Sep. 2008, doi: 10.1007/s00775-008-0395-2.
[10] G. J. Palm et al., “Specific binding of divalent metal ions to tetracycline and to the Tet repressor/tetracycline complex,” Journal of Biological Inorganic Chemistry, vol. 13, no. 7, pp. 1097–1110, Sep. 2008, doi: 10.1007/s00775-008-0395-2.
[11] V. Uivarosi, “Metal complexes of quinolone antibiotics and their applications: An update,” Sep. 2013. doi: 10.3390/molecules180911153.
[12] A. Tripathi, P. Suriyamoorthy, and A. Rawson, “Nitrofuran residues in animal sourced food: Sample extraction and identification methods – A review,” Dec. 01, 2023, Elsevier Ltd. doi: 10.1016/j.focha.2023.100396.
[13] S. Zhi et al., “Simultaneous extraction and determination of 45 veterinary antibiotics in swine manure by liquid chromatography-tandem mass spectrometry,” J Chromatogr B Analyt Technol Biomed Life Sci, vol. 1154, Oct. 2020, doi: 10.1016/j.jchromb.2020.122286.
[14] C. Poindexter, A. Yarberry, C. Rice, and S. Lansing, “Quantifying Antibiotic Distribution in Solid and Liquid Fractions of Manure Using a Two-Step, Multi-Residue Antibiotic Extraction,” Antibiotics, vol. 11, no. 12, Dec. 2022, doi: 10.3390/antibiotics11121735.
[15] A. Tripathi, P. Suriyamoorthy, and A. Rawson, “Nitrofuran residues in animal sourced food: Sample extraction and identification methods – A review,” Dec. 01, 2023, Elsevier Ltd. doi: 10.1016/j.focha.2023.100396.
Việt Nguyễn là đại lý chính thức sản phẩm Sắc ký lỏng khối phổ LC-MS/MS hãng SCIEX tại Việt Nam
Quý khách hàng cần hỗ trợ tư vấn, xin liên hệ Việt Nguyễn thông tin sau:
| CÔNG TY TNHH THƯƠNG MẠI – DỊCH VỤ – KỸ THUẬT VIỆT NGUYỄN | |
| Địa chỉ | VPHCM: số N36, đường số 11, P. Tân Thới Nhất, Q.12, Tp. Hồ Chí Minh. VPHN: Tòa Intracom, Số 33 Cầu Diễn, Phường Cầu Diễn, Quận Nam Từ Liêm, Hà Nội. VPĐN: Số 10 Lỗ Giáng 5, phường Hòa Xuân, quận Cẩm Lệ, Tp. Đà Nẵng. |
| Liên hệ | 0817 663300 (Mr.Hiếu) – E: hieu@vietnguyenco.vn |
| info@vietnguyenco.vn | |
| Website | https://www.vietcalib.vn| https://vietnguyenco.vn |